熱線:021-56056830,66110819
手機:13564362870


熱線:021-56056830,66110819
手機:13564362870
3.3納米材料組裝界面
納米材料組裝界面一般通過改變界面處的傳質來提高生物傳感器的便捷性。BESANT等開發了納米材料微電極,用于研究生物傳感器的靈敏度;他們通過在硅片上制備電沉積后組裝巰基適配體來制備納米材料微電極,并進行分子動力學模擬,證實了納米材料微電極可以抑制適配體聚集,并增加界面傳質,從而提高適配體的識別性能;該研究結果顯示,納米材料微電極適配體傳感器的靈敏度與普通電極相比,提高了10 000倍;并發現納米材料微電極傳感器的超高靈敏度具有很多優勢,如可以在30 min內檢測到細菌的RNA。基于納米材料微電極的適配體檢測平臺可用于檢測一系列生物標志物,包括病原抗菌藥物耐藥性標志物和腫瘤生物標志物。
3.4基于框架核酸的組裝界面
框架核酸的中空結構使空間能夠被最大化利用,非常適合在界面處組裝,可以提供具有低成本和高重現性的高分辨率的界面。適配體連接的框架核酸錨定到界面上,可用于生物傳感的開發。PEI等在框架核酸的頂部連上1個適配體,結果顯示,凝血酶與適配體形成了穩定的夾層結構,這一方法可用來特異性檢測凝血酶。類似的方法也可以應用于其他標志物的檢測。
4適配體傳感器在生物標志物檢測中的應用
4.1用于腫瘤生物標志物檢測
目前,適配體生物傳感器已被用于各種腫瘤生物標志物、抗原和細胞的檢測,如人類表皮生長因子受體2、血管內皮生長因子、表皮生長因子受體、PDGF黏液蛋白1、前列腺特異性抗原和癌胚抗原。
4.1.1抗原類生物標志物檢測過去幾十年,基于適配體的生物傳感器因其良好的靈敏度和選擇性、快速響應和低成本等優點,被廣泛應用于低濃度抗原類標志物的檢測。癌胚抗原(carcinoembryonic antigen,CEA)是在胚胎內胚層上皮中發現的潛在生物標志物,一般用于監測結直腸癌的治療效果,以及輔助診斷乳腺癌、胃腸道腫瘤、肝癌、肺癌、卵巢癌和胰腺癌。MAZLOUM-ARDAKANI等開發了一種基于多壁碳納米管、血紅素和石墨烯納米片的電化學適配體傳感器,用于檢測CEA,線性范圍為1.0×10-15~1.0×10-8g/mL,檢測限為0.82 fg/mL;檢測原理為納米復合材料多壁碳納米管可提高導電性,并加速血紅素和電極之間的電子轉移,當CEA結合適配體時,血紅素的信號會進一步降低。這種低成本、高靈敏度和特異性的生物傳感器在臨床樣本CEA檢測中有較大的應用價值。見圖1。
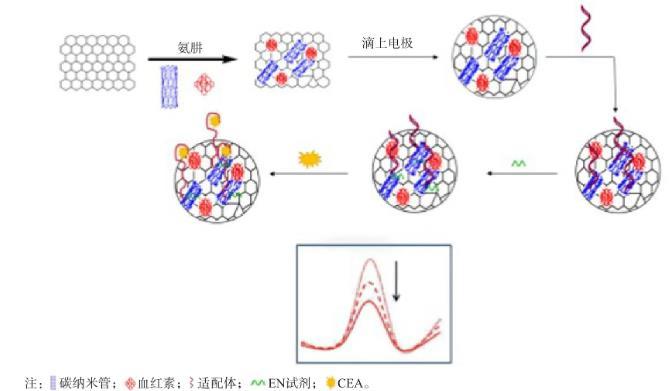
圖1用于檢測CEA的適配體傳感器的制備和工作示意圖
4.1.2循環腫瘤細胞檢測
循環腫瘤細胞由原發腫瘤組織脫落后,可進入血液循環和淋巴循環,因其在腫瘤轉移早期階段出現,已成為癌癥監測和診斷的重要生物標志物。YANG等開發了一種DNA標記夾心電化學生物傳感器,基于3D石墨烯和金納米籠/氨基化多壁碳納米管混合物,采用差分脈沖伏安法檢測乳腺癌細胞MCF-7;由于納米材料具有放大信號的優勢,這種電化學傳感器檢測MCF-7細胞時表現出高特異性和高靈敏度的優勢,檢測范圍為1.0×102~1.0×106個/mL,檢測限低至80個/mL。這種方法具有很大的實際應用潛力,在癌癥診斷中具有較好的前景。
4.1.3外泌體檢測
外泌體是一種細胞外囊泡,直徑為30~150 nm,可以調節腫瘤微環境,被認為是最重要的腫瘤生物標志物之一。
ZHOU等將適配體固定在電極的表面,在互補適配體的一端修飾電活性物質亞甲藍,當目標外泌體存在時,CD63適配體可以識別外泌體上的CD63蛋白膜,電活性物質在電極上的電信號發生改變,從而實現外泌體的檢測。見圖2。
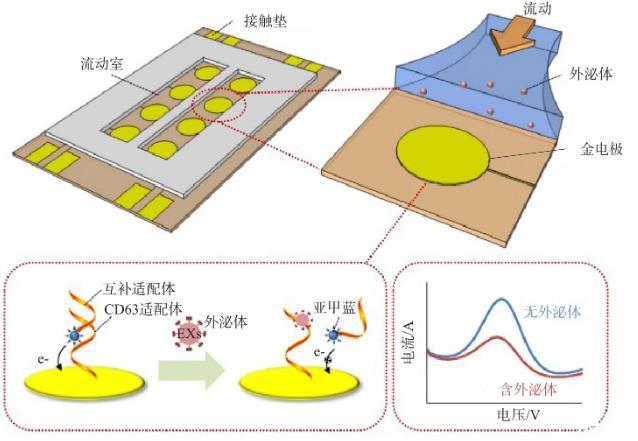
圖2基于適配體檢測外泌體的示意圖
4.2用于心血管疾病生物標志物檢測
心血管疾病是人類健康的最大威脅,具有高患病率、高致殘率和高死亡率的特點。開發操作簡單、靈敏、低成本的心血管疾病生物標志物傳感器非常必要。QIAO等開發了基于適配體-MoS2納米共軛物的電化學傳感器,用于檢測心肌肌鈣蛋白I,并與基于Au SiO2 Au納米顆粒的電化學傳感器的檢測效能進行比較,結果顯示,2種傳感器均可以檢測人血液樣本中的心肌肌鈣蛋白I,但基于適配體-MoS2納米共軛物的電化學傳感器檢測心肌肌鈣蛋白I的線性范圍為10 pmol/L~1.0μmol/L,檢測限為0.95 pmol/L,較適配體Au SiO2 Au傳感器具有更低的檢測限;此外,在不含有肌酸激酶MB同工酶和肌紅蛋白的樣本中,2種傳感器均表現出良好的診斷效能。